
下载APP

【简答题】


工业上用含锌物料(含FeO、CuO等杂质)可制得活性ZnO,流程如下:
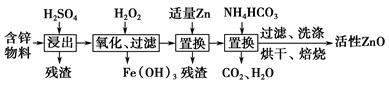 (1)上述流程中,浸出用的是60%H 2SO 4(1.5 g·cm -3),配制这种H 2SO 4 100 mL需要18.4 mol·L -1的浓H 2SO 4________ mL(保留一位小数)。 (2)加入氧化剂H 2O 2后,有Fe(OH) 3沉淀出现,没有Cu(OH) 2沉淀出现,若溶液中c(Fe 3 +)=2.6×10 -18 mol·L -1,则溶液中c(Cu 2 +)的取值范围是________mol·L -1。(已知K sp[Fe(OH) 3]=2.6×10 -39, K sp[Cu(OH) 2]=2.2×10 -20) (3)加入NH 4HCO 3后生成的沉淀是形态均为Zn a(OH) b(CO 3) c(a、b、c为)的两种碱式碳酸锌A和B的混合物,A中a=5、b=6,则生成碱式碳酸锌A的化学方程式为__________________________________________________。 (4)取洗涤、烘干后的碱式碳酸锌A和B的混合物49.70 g,其物质的量为0.10 mol,高温焙烧完全分解得到37.26 g ZnO、3.584 L CO 2(标准状况下)和水,通过计算求出碱式碳酸锌B的化学式。
(1)上述流程中,浸出用的是60%H 2SO 4(1.5 g·cm -3),配制这种H 2SO 4 100 mL需要18.4 mol·L -1的浓H 2SO 4________ mL(保留一位小数)。 (2)加入氧化剂H 2O 2后,有Fe(OH) 3沉淀出现,没有Cu(OH) 2沉淀出现,若溶液中c(Fe 3 +)=2.6×10 -18 mol·L -1,则溶液中c(Cu 2 +)的取值范围是________mol·L -1。(已知K sp[Fe(OH) 3]=2.6×10 -39, K sp[Cu(OH) 2]=2.2×10 -20) (3)加入NH 4HCO 3后生成的沉淀是形态均为Zn a(OH) b(CO 3) c(a、b、c为)的两种碱式碳酸锌A和B的混合物,A中a=5、b=6,则生成碱式碳酸锌A的化学方程式为__________________________________________________。 (4)取洗涤、烘干后的碱式碳酸锌A和B的混合物49.70 g,其物质的量为0.10 mol,高温焙烧完全分解得到37.26 g ZnO、3.584 L CO 2(标准状况下)和水,通过计算求出碱式碳酸锌B的化学式。
参考答案:


参考解析:




刷刷题刷刷变学霸
举一反三

【单选题】下列各组热化学方程式中,化学反应的△H前者大于后者的是( ) ①C(g)+O 2 (g )═CO 2 (g),△H 1 ; C(g)+ 1 2 O 2 (g)═CO(g ),△H 2 ; ②S(s)+O 2 (g )═SO 2 (g),△H 3 ; S(g)+O 2 (g)═SO 2 (g),△H 4 ; ③H 2 (g)+ 1 2 O 2 (g )═H 2 O(l),△...
A.
①②③
B.
②③④
C.
④
D.
①
【单选题】已知热化学方程式:SO 2(g)+ O 2(g) SO 3(g) △H =" ―98.32" kJ/mol,在容器中充入2molSO 2 和1molO 2充分反应,最终放出的热量为
A.
196.64kJ
B.
196.64kJ/mol
C.
<196.64kJ
D.
>196.64kJ
【单选题】下列叙述中正确的是( )已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下:H2(g)+Cl2(g)=2HCl(g);△H=-Q1kJ/molH2(g)+Br2(g)=2HBr(g);△H=-Q2kJ/mol下列叙述中正确的是( )
A.
Q1<Q2
B.
生成物总能量均高于反应物总能量
C.
生成1molHCl气体时放出Q1热量
D.
1molHBr(g)具有的能量大于1molHBr(l)具有的能量
【判断题】根据实际情况,现场多储备碱式碳酸锌[Zn2(OH)2CO3],其为白色粉末,密度为4.4 g/cm3,很难溶于水中(0.03%~0.05%),其组成不定,在140 ℃即分解,形成ZnO、CO2和H2O。
A.
正确
B.
错误
【单选题】下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa): ① ② ③ ④ 由此判断,正丁烷的燃烧热是______。
A.
-2878kJ/mol
B.
-2658kJ/mol
C.
-1746kJ/mol
D.
-1526kJ/mol

