
下载APP

【简答题】


水钴矿中除SiO 2外,还有9.24% CoO、2.78% Fe 2O 3、0.96% MgO、0.084 % 。从中提取钴的主要工艺流程如下:
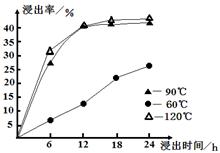
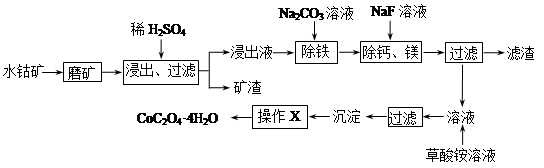 (1)在一定浓度的H 2SO 4溶液中,钴的浸出率随时间、温度的变化如图所示。考虑生产成本和效率,最佳的浸出时间为 小时,最佳的浸出温度为 ℃。
(1)在一定浓度的H 2SO 4溶液中,钴的浸出率随时间、温度的变化如图所示。考虑生产成本和效率,最佳的浸出时间为 小时,最佳的浸出温度为 ℃。
 (2)请配平下列除铁的化学方程式: Fe 2(SO 4) 3+ H 2O+ Na 2CO 3= Na 2Fe 6(SO 4) 4(OH) 12↓+ Na 2SO 4+ CO 2↑ (3)“除钙、镁”的原理反应为:MgSO 4+2NaF=MgF 2↓+Na 2SO 4 ;CaSO 4+2NaF=CaF 2↓+Na 2SO 4 已知K sp(CaF 2)=1.11×10 -10,K sp(MgF 2)=7.40×10 -11,加入过量NaF溶液反应完全后过滤,则滤液中
(2)请配平下列除铁的化学方程式: Fe 2(SO 4) 3+ H 2O+ Na 2CO 3= Na 2Fe 6(SO 4) 4(OH) 12↓+ Na 2SO 4+ CO 2↑ (3)“除钙、镁”的原理反应为:MgSO 4+2NaF=MgF 2↓+Na 2SO 4 ;CaSO 4+2NaF=CaF 2↓+Na 2SO 4 已知K sp(CaF 2)=1.11×10 -10,K sp(MgF 2)=7.40×10 -11,加入过量NaF溶液反应完全后过滤,则滤液中
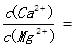 。 (4)“沉淀”中含杂质离子主要有SO 4 2 -、F -、 和 ;“操作X”包括 和 。 (5)某锂离子电池正极是LiCoO 2,含Li +导电固体为电解质。充电时,Li +还原为Li,并以原子形式嵌入电池负极材料碳-6(C 6)中(如图所示)。电池反应为LiCoO 2+C 6
。 (4)“沉淀”中含杂质离子主要有SO 4 2 -、F -、 和 ;“操作X”包括 和 。 (5)某锂离子电池正极是LiCoO 2,含Li +导电固体为电解质。充电时,Li +还原为Li,并以原子形式嵌入电池负极材料碳-6(C 6)中(如图所示)。电池反应为LiCoO 2+C 6
 CoO 2+LiC 6,写出该电池放电时的正极反应式 。
CoO 2+LiC 6,写出该电池放电时的正极反应式 。

参考答案:


参考解析:




刷刷题刷刷变学霸
举一反三

【单选题】下列各组热化学方程式中,化学反应的△H前者大于后者的是( ) ①C(g)+O 2 (g )═CO 2 (g),△H 1 ; C(g)+ 1 2 O 2 (g)═CO(g ),△H 2 ; ②S(s)+O 2 (g )═SO 2 (g),△H 3 ; S(g)+O 2 (g)═SO 2 (g),△H 4 ; ③H 2 (g)+ 1 2 O 2 (g )═H 2 O(l),△...
A.
①②③
B.
②③④
C.
④
D.
①
【单选题】已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是( )
A.
N2H4+O2=N2+2H2O△H= —534.4kJ/mol
B.
N2H4(g)+ O2(g)=N2(g)+2H2O(g)△H = —16.7kJ/mol
C.
N2H4(g)+O2(g)=N2(g)+2H2O(l)△H = —534.4kJ/mol
D.
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H = —534.4kJ/mol
【单选题】已知热化学方程式:SO 2(g)+ O 2(g) SO 3(g) △H =" ―98.32" kJ/mol,在容器中充入2molSO 2 和1molO 2充分反应,最终放出的热量为
A.
196.kJ
B.
196.kJ/mol
C.
<196.kJ
D.
>196.kJ
【单选题】下列叙述中正确的是( )已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下:H2(g)+Cl2(g)=2HCl(g);△H=-Q1kJ/molH2(g)+Br2(g)=2HBr(g);△H=-Q2kJ/mol下列叙述中正确的是( )
A.
Q1<Q2
B.
生成物总能量均高于反应物总能量
C.
生成1molHCl气体时放出Q1热量
D.
1molHBr(g)具有的能量大于1molHBr(l)具有的能量
【多选题】锂离子电池的工作原理是
A.
充电时,正极的Li+从化合物中脱出,经电解液输运到负极碳材料中嵌入;
B.
充电时,负极的Li+从化合物中脱出,经电解液输运到正极碳材料中嵌入;
C.
放电时,潜在正极的碳材料的Li+脱嵌,回到负极形成锂化合物;
D.
放电时,潜在负极的碳材料的Li+脱嵌,回到正极形成锂化合物;
【单选题】将CO2和H2以一定比例混合,在一定条件下反应生成一种重要的化工原料X和水,其反应的化学方程式为:CO2 + 3H2 =X + H2O。下列有关这个反应的说法中不正确的是( )
A.
X是有机化合物
B.
X的化学式为CH4O
C.
该反应为置换反应
D.
这个反应开辟了二氧化碳的一个新用途
【单选题】已知1 mol CH4气体完全燃烧生成气态CO2和液态H2O,放出890.3 kJ热量,则表示该反应的热化学方程式正确的是
A.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) Δ H =+ 890.3 kJ · mol ˉ 1
B.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) Δ H =- 890.3 kJ · mol ˉ 1
C.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) Δ H =+ 890.3 kJ · mol ˉ 1
D.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) Δ H =- 890.3 kJ · mol ˉ 1
【单选题】下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa): ① ② ③ ④ 由此判断,正丁烷的燃烧热是______。
A.
-2878kJ/mol
B.
-2658kJ/mol
C.
-1746kJ/mol
D.
-1526kJ/mol
相关题目:

【单选题】已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是( )
A.
N2H4+O2=N2+2H2O△H= —534.4kJ/mol
B.
N2H4(g)+ O2(g)=N2(g)+2H2O(g)△H = —16.7kJ/mol
C.
N2H4(g)+O2(g)=N2(g)+2H2O(l)△H = —534.4kJ/mol
D.
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H = —534.4kJ/mol
【单选题】已知热化学方程式:SO 2(g)+ O 2(g) SO 3(g) △H =" ―98.32" kJ/mol,在容器中充入2molSO 2 和1molO 2充分反应,最终放出的热量为
A.
196.kJ
B.
196.kJ/mol
C.
<196.kJ
D.
>196.kJ
【单选题】下列叙述中正确的是( )已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下:H2(g)+Cl2(g)=2HCl(g);△H=-Q1kJ/molH2(g)+Br2(g)=2HBr(g);△H=-Q2kJ/mol下列叙述中正确的是( )
A.
Q1<Q2
B.
生成物总能量均高于反应物总能量
C.
生成1molHCl气体时放出Q1热量
D.
1molHBr(g)具有的能量大于1molHBr(l)具有的能量
【多选题】锂离子电池的工作原理是
A.
充电时,正极的Li+从化合物中脱出,经电解液输运到负极碳材料中嵌入;
B.
充电时,负极的Li+从化合物中脱出,经电解液输运到正极碳材料中嵌入;
C.
放电时,潜在正极的碳材料的Li+脱嵌,回到负极形成锂化合物;
D.
放电时,潜在负极的碳材料的Li+脱嵌,回到正极形成锂化合物;
【单选题】将CO2和H2以一定比例混合,在一定条件下反应生成一种重要的化工原料X和水,其反应的化学方程式为:CO2 + 3H2 =X + H2O。下列有关这个反应的说法中不正确的是( )
A.
X是有机化合物
B.
X的化学式为CH4O
C.
该反应为置换反应
D.
这个反应开辟了二氧化碳的一个新用途
【单选题】已知1 mol CH4气体完全燃烧生成气态CO2和液态H2O,放出890.3 kJ热量,则表示该反应的热化学方程式正确的是
A.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) Δ H =+ 890.3 kJ · mol ˉ 1
B.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) Δ H =- 890.3 kJ · mol ˉ 1
C.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) Δ H =+ 890.3 kJ · mol ˉ 1
D.
CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) Δ H =- 890.3 kJ · mol ˉ 1
【单选题】下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa): ① ② ③ ④ 由此判断,正丁烷的燃烧热是______。
A.
-2878kJ/mol
B.
-2658kJ/mol
C.
-1746kJ/mol
D.
-1526kJ/mol

