
下载APP

【简答题】


工业上常用一定浓度的稀硫酸对表面生锈的铁件进行酸洗。某酸洗池里盛有440Kg质量分数为40%的硫酸溶液,放入表面生锈的铁件浸泡,浸泡过程中单质铁也有部分损失,假设溶液中只发生如下反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O;Fe+Fe2(SO4)3==3FeSO4。
取出铁件用水冲洗,冲洗液倒入酸洗池中合并共得到580Kg溶液,其中只有H2SO4和FeSO4两种溶质,经过测定硫酸的质量分数降低到5%。计算:
⑴消耗硫酸的质量
⑵损失的单质铁的质量
⑶要使硫酸的质量分数恢复到40%,需要加入质量分数为98%的浓硫酸的质量。
参考答案:


参考解析:




刷刷题刷刷变学霸
举一反三

【单选题】甲乙两烧杯中分别盛有等体积、等浓度的硫酸溶液.向甲杯中放入m克镁,向乙杯中投入m克锌.完全反应后发现有一烧杯中金属有剩余.则各杯中原来硫酸的质量x之值是 [ ]
A.
x=
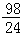 m克
m克
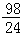 m克
m克B.
 m>x>
m>x>
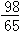 m
m
 m>x>
m>x>
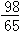 m
mC.
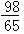 m>x≥
m>x≥
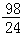 m
m
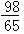 m>x≥
m>x≥
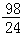 m
mD.
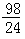 m>x≥
m>x≥
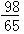 m
m
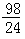 m>x≥
m>x≥
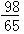 m
m【单选题】C(H2SO4)0.1mol/L硫酸溶液100mL中所含H2SO4质量为()。(注:H2SO4分子量为98)
A.
4.9克
B.
9.88克
C.
0.49克
D.
0.98克

