
下载APP

【简答题】


(12分) KClO 3在农业上用作除草剂,超细CaCO 3泛用于消光纸、无炭复写纸等。某同学在实验室模拟工业过程,利用制乙炔产生的残渣制备上述两种物质,过程如下: I.
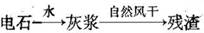 ①电石与水反应的化学方程式是__________。 ②残渣中主要成分是Ca(OH) 2和________。 II.将I中的部分灰浆配成池液,通人Cl 2,得到Ca(Clo 3) 2与Cacl 2物质的量之比为1:5的溶液,反应的化学方程式是________________ III.向II所得溶液中加人KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO 3晶体。你认为能得到KClO 3晶体的原因是________________。 IV.将I中的残渣溶于NH 4Cl溶液,加热,收集挥发出的气体再利用。向所得CaCl 2溶液中依次通入NH 3、C0 2,便可获得超细CaCO 3,过程如下:
①电石与水反应的化学方程式是__________。 ②残渣中主要成分是Ca(OH) 2和________。 II.将I中的部分灰浆配成池液,通人Cl 2,得到Ca(Clo 3) 2与Cacl 2物质的量之比为1:5的溶液,反应的化学方程式是________________ III.向II所得溶液中加人KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO 3晶体。你认为能得到KClO 3晶体的原因是________________。 IV.将I中的残渣溶于NH 4Cl溶液,加热,收集挥发出的气体再利用。向所得CaCl 2溶液中依次通入NH 3、C0 2,便可获得超细CaCO 3,过程如下:
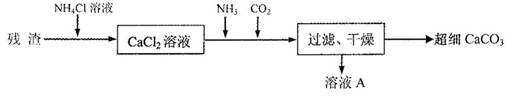 ①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因________。 ②CaCl 2溶液中通入两种气体后,生成超细CaCO 3的化学方程式是________。 ③图示的溶液A可循环使用,其主要成分的化学式是________
①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因________。 ②CaCl 2溶液中通入两种气体后,生成超细CaCO 3的化学方程式是________。 ③图示的溶液A可循环使用,其主要成分的化学式是________
参考答案:


参考解析:




刷刷题刷刷变学霸
举一反三

【单选题】下列叙述中正确的是( )已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下:H2(g)+Cl2(g)=2HCl(g);△H=-Q1kJ/molH2(g)+Br2(g)=2HBr(g);△H=-Q2kJ/mol下列叙述中正确的是( )
A.
Q1<Q2
B.
生成物总能量均高于反应物总能量
C.
生成1molHCl气体时放出Q1热量
D.
1molHBr(g)具有的能量大于1molHBr(l)具有的能量
【单选题】将硫酸锌溶液蒸发浓缩,冷却后的产物是( ) 。
A.
ZnSO 4
B.
ZnSO 4 ·10H 2 O
C.
ZnSO 4 ·5H 2 O
D.
ZnSO 4 ·7H 2 O
【单选题】下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa): ① ② ③ ④ 由此判断,正丁烷的燃烧热是______。
A.
-2878kJ/mol
B.
-2658kJ/mol
C.
-1746kJ/mol
D.
-1526kJ/mol

