
下载APP

化学平衡的有关计算题库

题数
2000
考试分类
高中化学>化学平衡的有关计算
售价
¥30
收藏
分享
去刷题



章节目录
简介
高中化学-化学平衡的有关计算
...更多
题目预览
【简答题】

[1/2000]2.0 mol PCl 3和1.0 mol Cl 2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl 3(g)+Cl 2(g) 【图片】 P...
参考答案:
|
B
|
参考解析:
考查化学平衡的移动及等效平衡
依据所给信息可知,当平衡时再加入1.0 mol PCl 3和0.50 mol Cl 2时,相当于另一个初始状态:3.0 mol PCl 3和1.5 mol Cl 2充入体积不变的密闭容器中;
我们可以这样理解:该初始状态的容器体积为1.5倍的原容器体积,那么平衡时,PCl 5的物质的量一定为0.40×1.5="0.60" mol,再压缩至原容器体积,平衡正向移动,PCl 5的物质的量增大,必定大于0.60 mol
依据所给信息可知,当平衡时再加入1.0 mol PCl 3和0.50 mol Cl 2时,相当于另一个初始状态:3.0 mol PCl 3和1.5 mol Cl 2充入体积不变的密闭容器中;
我们可以这样理解:该初始状态的容器体积为1.5倍的原容器体积,那么平衡时,PCl 5的物质的量一定为0.40×1.5="0.60" mol,再压缩至原容器体积,平衡正向移动,PCl 5的物质的量增大,必定大于0.60 mol
【简答题】

[2/2000]在一定温度下、一定体积的密闭容器中有如下平衡:H 2(g)+I 2(g) 【图片】2HI(g)。已知H 2和I 2的起始浓度均为0.10 mol/L,...
参考答案:
|
D
|
参考解析:
无
【简答题】

[3/2000]在一定条件下,向一固定容积的容器中投入2molNO2进行反应:2NO2 【图片】2NO+O2,一段时间后测得NO2、NO、O2的物质的量可能是 [&n...
参考答案:
| D |
参考解析:
无
【简答题】

[4/2000]a 1和a 2分别为A在两个恒容容器中平衡体系A(g) 【图片】2B(g) 和2A(g) 【图片】B(g)的转化率,在温度不变的情况下,均增加A的物质...
参考答案:
|
D
|
参考解析:
无
【简答题】

[5/2000]某反应中,X、Y、Z三种物质的物质的量随时间的变化如图所示。下列说法正确的是 【图片】A.反应为 X + 2Z= YB.反应为 X + Y 【图片】2...
参考答案:
|
B
|
参考解析:
根据图像可知,X、Y的物质的量减少,Z的物质的量增加,说明X、Y是反应物,Z是生成物。反应进行到10min时,物质到浓度不再发生变化,说明反应达到平衡状态,所以选项C不正确。平衡时反应速率不等于0,选项D不正确。平衡时X和Y分别减少了1.20mol-0.40mol=0.80mol、1.00mol-0.20mol=0.80mol,Z增加了1.60mol。根据变化量之比是相应的化学计量数之比可知,反应的化学方程式是X + Y
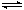 2Z,B正确,A不正确,答案选B。
2Z,B正确,A不正确,答案选B。
点评:该题是中等难度的试题,试题贴近高考,基础性强,有利于培养学生的逻辑推理能力和发散思维能力。答题时注意根据图中物质的变化确定反应物和生成物,并能依据变化量之比是相应的化学计量数之比进行计算。
【简答题】

[6/2000](原创题)某温度下,反应2NO 2(g) 【图片】N 2O 4(g) ΔH<0在密闭容器中达到平衡,下列叙述中正确的是 &...
参考答案:
|
A
|
参考解析:
无
【简答题】

[7/2000]下列反应中可判断为可逆反应的是( ) A.氢气和氯气点燃生成氯化氢,氯化氢受热分解为氢气和氯气B.氮气和氢气在高温、高压、催化剂作用下可以生成氨气...
参考答案:
|
B
|
参考解析:
无
【简答题】

[8/2000](18分)铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。 Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH 4) 2SO 4溶液。...
参考答案:
|
(18分)
Ⅰ(1)d e f (2分) (2)氢氧化钠电离出的OH -增大了氨水中OH -浓度,促使氨水电离平衡NH 3+H 2O  NH
4
++OH
—左移,有利氨气逸出。(2分) NH
4
++OH
—左移,有利氨气逸出。(2分)
(3) 分液(2分)。 (4)密封、阴凉、通风(2分) Ⅱ(1)Mg(OH) 2+NH 4Cl  MgOHCl+NH
3↑+H
2O(2分) MgOHCl+NH
3↑+H
2O(2分)
(2)防止装置C中的AlCl 3溶液倒吸入装置B(2分) (3)a(2分) (4)①用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色火焰产生,则证明所得无水氯化镁晶体中不含氯化钠。(2分)(答焰色反应也给分) ②HCl(气流)(2分) |
参考解析:
Ⅰ(1)制取的氨气与硫酸反应生成硫酸铵,剩余的氨气用水吸收,故连接顺序为a→d→e→f。
(2)氨水中存在电离平衡: NH 3+H 2O
 NH
4
++OH
—,与NaOH混合后,NaOH电离出OH
-,促使氨水电离平衡向左移动,有利氨气逸出。
NH
4
++OH
—,与NaOH混合后,NaOH电离出OH
-,促使氨水电离平衡向左移动,有利氨气逸出。
(3)分离互不相溶的液体的方法是:分液。
(4)因为(NH 4) 2SO 4“低毒,有刺激性,有吸湿性、吸湿后固结成块”,应防止水分进入,所以储存应注意密封、阴凉、通风。
Ⅱ(1)根据题目所给信息,反应物为Mg(OH) 2和NH 4Cl,生成物为MgOHCl、NH 3和H 2O,所以化学方程式为:Mg(OH) 2+NH 4Cl
 MgOHCl+NH
3↑+H
2O。
MgOHCl+NH
3↑+H
2O。
(2)防止装置C中的AlCl 3溶液倒吸入装置B
(3)由MgCl 2溶液得到MgCl 2·6H 2O晶体的方法为蒸发浓缩、降温结晶,所以蒸发的目的是:得到热饱和溶液,故a项正确。
(4)①Na元素用焰色反应进行鉴别,所以操作方法是:用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色火焰产生,则证明所得无水氯化镁晶体中不含氯化钠。
②因为MgCl 2为强酸弱碱盐,Mg 2+发生水解反应,在HCl(气流)中可以抑制MgCl 2的水解,所以由MgCl 2·6H 2O制备无水MgCl 2的操作在HCl氛围中进行。
【简答题】

[9/2000]在一密闭容器中,反应 aA(g) 【图片】 bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度变为...
参考答案:
|
D
|
参考解析:
反应 aA(g)
 bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,若平衡不发生移动,则由于体系的体积是原来的2倍,所以浓度是原来的一半,现在最终测得A的物质的量的浓度变为原来的50%,所以该反应为反应前后气体的体积相等的反应。改变压强化学平衡不发生移动,a=(b+c)。反应体系中任何物质的浓度由于平衡未发生移动,都不变。因此选项中的各种说法都错误。选项为D。
bB(g)+cC(g)达平衡后,保持温度不变,将容器体积增加一倍,若平衡不发生移动,则由于体系的体积是原来的2倍,所以浓度是原来的一半,现在最终测得A的物质的量的浓度变为原来的50%,所以该反应为反应前后气体的体积相等的反应。改变压强化学平衡不发生移动,a=(b+c)。反应体系中任何物质的浓度由于平衡未发生移动,都不变。因此选项中的各种说法都错误。选项为D。
【简答题】

[10/2000]把2.5mol A和2.5mol B混合盛入2L容积的密闭容器里发生反应3A(g)+B(g)⇌x C(g)+2D(g),...
参考答案:
| (1)5s内C的平均反应速率为0.2mol•L-1•s-1,同时生成1molD,故生成的C的物质的量为5s×0.2mol•L-1•s-1×2L=2mol,化学计量数之比等于物质的量之比,故x:2=2mol:1mol,解得x=4, 答:x的值为4; (2)由方程式3A(g)+B(g)⇌4C(g)+2D(g)可知,参加反应的B的物质的量为1mol×
答:平衡时B的转化率为20%; (3)0.5molB反应放出的热量为QkJ,故1molB反应放出的热量为QkJ×
答:该反应的热化学方程式为3A(g)+B(g)⇌4 C(g)+2D(g)△H=-2Q kJ•mol-1; (4)反应生成1molD,则: 3A(g)+B(g)⇌4 C(g)+2D(g) 气体物质的量增大△n 2 2 1mol 1mol 故平衡时混合气体的物质的量为2.5mol+2.5mol+1mol=6mol,恒温恒压下,体积之比之比等于物质的量之比,令平衡时的体积为V,则5mol:6mol=2L:V,解得V=2.4L, 答:达平衡时容器内气体的体积为2.4L. |
参考解析:
12