
下载APP

氧化铁题库

题数
1106
考试分类
高中化学>氧化铁
售价
¥30
收藏
分享
去刷题



章节目录
简介
高中化学-氧化铁
...更多
题目预览
【简答题】

[1/1106]日本地震后,导致福岛第一核电站引发核危机。核反应堆的第一层护罩是锆锡合金外壳,第二层护罩是压力仓,第三层护罩是用最坚固的钢和混凝土制成的非常厚的球体。...
参考答案:
|
B
|
参考解析:
钢是铁碳合金,其硬度大于纯铁,但熔点低于纯铁。
【简答题】

[2/1106]铁及铁的化合物应用广泛,如FeCl 3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。 (1)写出FeCl 3溶液腐蚀印刷电路铜板的离子方程式____...
参考答案:
|
(1)2Fe
3
++Cu=2Fe
2
++Cu
2
+
(2)装置图如图所示 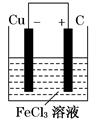
正极反应:2Fe 3 ++2e -=2Fe 2 + 负极反应:Cu-2e -=Cu 2 + |
参考解析:
(1)利用Fe
3
+氧化性的反应:2FeCl
3+Cu=2FeCl
2+CuCl
2,然后改为离子方程式。
(2)根据2Fe 3 ++Cu=2Fe 2 ++Cu 2 +氧化还原反应和原电池的工作原理进行设计,铜作负极,石墨作正极,FeCl 3溶液作电解质溶液。
(2)根据2Fe 3 ++Cu=2Fe 2 ++Cu 2 +氧化还原反应和原电池的工作原理进行设计,铜作负极,石墨作正极,FeCl 3溶液作电解质溶液。
【简答题】

[3/1106](3分) 某金属X,为了确定其成分,进行一系列实验,实验过程和发生的现象如下图所示: 【图片】⑴写出金属X的化学式 ...
参考答案:
|
⑴ Fe 。⑵ FeCl
2 。
⑶ 4Fe(OH) 2+O 2+2H 2O=4Fe(OH) 3。(2分) |
参考解析:
略
【简答题】

[4/1106]某混合液中含有等物质的量的CuSO 4、FeSO 4、Fe 2(SO 4) 3。已知下表数据:下列叙述正确的是 物质(25℃)Cu(OH)2Fe(OH...
参考答案:
|
D
|
参考解析:
试题分析:A、由于在溶液中Cu 2 +、Fe 3 +、Fe 2 +均要水解,因此混合溶液中c(SO 4 2 -):[ c(Cu 2 +) +c(Fe 3 +) +c(Fe 2 +)]>5:4,A不正确;B、铁是活泼的金属,能置换出铜,因此只有铁足量能观察到红色固体析出,B不正确;C、若向混合溶液中加入足量氯水,则硫酸亚铁被氧化生成硫酸铁,然后调节pH到3~4后氢氧化铁完全沉淀,过滤后所得溶液应该是硫酸铜、硫酸和氯水的混合液,得不到纯净的CuSO 4溶液,C不正确;D、根据溶度积常数可知,以及Cu(OH) 2、Fe(OH) 2、Fe(OH) 3完全沉淀时的pH值可知,若向混合溶液中逐滴加入烧碱溶液,首先生成Fe(OH) 3沉淀,D正确,答案选D。
【简答题】

[5/1106]为了检验FeCl 2溶液是否氧化变质,可向溶液中加入的试剂是( ) A.盐酸B.KSCN溶液C.氯水D....
参考答案:
|
B
|
参考解析:
A.FeCl 2 、FeCl 3都不与盐酸反应,所以不能检验是否变质,故A错误。
B.如果FeCl 2溶液变质,变质后的物质是FeCl 3,Fe 3+能和SCN -生成络合物,使溶液呈现血红色现象明显,这一反应是Fe 3+的特征反应,所以用KSCN溶液,故B正确。
C. FeCl 2被氯水氧化成氯化铁,也不能检验是否变质。
D、无论氯化亚铁是否变质,都是强酸弱碱盐,溶液都呈酸性,所以无法检验,故D错误.
故选:B
点评:检验Fe 3+的物质有:KSCN(溶液变血红色)、苯酚(溶液呈紫色)
【简答题】

[6/1106]把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe 2+和Fe 3+的浓度恰好相等。则已反应的Fe 3+和未反应的Fe 3+的物质的量之比为&...
参考答案:
|
C
|
参考解析:
Fe +2Fe 3+=3Fe 2+
1 2 3
从上述离子方程式得,若反应2molFe 3+(即已反应的Fe3+),生成3molFe 2+而所得溶液中Fe 2+和Fe 3+的溶度恰好相等,即未反应的Fe 3+的物质的量为3mol所以答案2:3,故选C。 3+和Fe 2+的转换的计算
点评:本题考查Fe 3+和Fe 2+的转换的计算,只需列出反应方程式,通过假设即可算出,不难理解。
【简答题】

[7/1106]某溶液中,Fe 3+、Cu 2+、Fe 2+的物质的量浓度之比为4:2:1,加入适量的铁粉,充分反应后,溶液中Fe 3+、Cu 2+、Fe 2+的物质...
参考答案:
|
B
|
参考解析:
假设原溶液中e
3+、Cu
2+、Fe
2+的物质的量分别是(mol)4、2、1,设投入的铁是x。则根据方程式2Fe
3
++Fe=3Fe
2
+可知消耗铁离子是2x,生成亚铁离子是3x,所以(4mol-2x)︰2︰(1mol+3x)=1:1:2,解得x=1,所以投入的铁粉与原溶液中Cu
2+的物质的量之比为1:2,答案选B。
【简答题】

[8/1106]FeCl 3、CuCl 2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是 A 加入KSCN溶液变红色 &nb...
参考答案:
|
AC
|
参考解析:
分阶段分析
①、当固体为铁、铜时,溶液中的Fe 3+、Cu 2+全部参加反应生成Fe 2+和Cu,反应的反应方程式为:2FeCl 3+Fe=3FeCl 2
CuCl 2+Fe=Cu+FeCl 2
所以溶液中一定没有Fe 3+、Cu 2+,一定含有Fe 2+;
②当固体为铜时,溶液中一定没有Fe 3+,Cu 2+恰好全部参加反应或部分反应生成Fe 2+和Cu,
所以溶液中一定没有Fe 3+,可能含有Cu 2+,一定含有Fe 2+;
A、溶液中一定不含Fe 3+,所以加入KSCN溶液不变红色,故A错误.
B、通过以上分析知,溶液中一定含有Fe 2+,故B正确.
C、通过以上分析知,溶液中可能含有Cu 2+,故C错误.
D、通过以上分析知,剩余固体中一定含Cu,故D正确.
故选A、C.
①、当固体为铁、铜时,溶液中的Fe 3+、Cu 2+全部参加反应生成Fe 2+和Cu,反应的反应方程式为:2FeCl 3+Fe=3FeCl 2
CuCl 2+Fe=Cu+FeCl 2
所以溶液中一定没有Fe 3+、Cu 2+,一定含有Fe 2+;
②当固体为铜时,溶液中一定没有Fe 3+,Cu 2+恰好全部参加反应或部分反应生成Fe 2+和Cu,
所以溶液中一定没有Fe 3+,可能含有Cu 2+,一定含有Fe 2+;
A、溶液中一定不含Fe 3+,所以加入KSCN溶液不变红色,故A错误.
B、通过以上分析知,溶液中一定含有Fe 2+,故B正确.
C、通过以上分析知,溶液中可能含有Cu 2+,故C错误.
D、通过以上分析知,剩余固体中一定含Cu,故D正确.
故选A、C.
【简答题】

[9/1106]过量的铁粉与稀硫酸反应后,溶液中存在较多的阳离子是 A.Fe3+B.Fe2+C.H+D.Fe3+和Fe2+
参考答案:
|
B
|
参考解析:
由于铁粉过量,故溶液中的H +几乎被消耗完,而铁粉与水反应会产生Fe 2+,故溶液中存在较多的阳离子是Fe 2+,由于铁粉过量故不存在Fe 3+。故答案选B
点评:本题需要学生对铁性质及Fe 2+与 Fe 3+互相转化的理解,但由于是过量的铁粉,所以三价不存在。
【简答题】

[10/1106]某同学设计如下实验测量 m g铜银合金样品中铜的质量分数: 【图片】下列说法中不正确的是 A.收集到的V L气体为 NOB.过滤用到的玻璃仪器是:烧杯...
参考答案:
|
D
|
参考解析:
铜和银与硝酸反应,生成NO
2或NO,但通过排水法收集到的气体是NO。溶液中加入氯化钠生成氯化银沉淀,即氯化银的质量是wg。所以根据原子守恒可知,合金中银的质量是
 ,则铜的质量分数为
,则铜的质量分数为
 ,即选项D是错误的,其余都是正确的,答案选D。
,即选项D是错误的,其余都是正确的,答案选D。
 ,则铜的质量分数为
,则铜的质量分数为
 ,即选项D是错误的,其余都是正确的,答案选D。
,即选项D是错误的,其余都是正确的,答案选D。